Článek
Musím se přiznat, že investice do biofarmaceutických firem mě nikdy příliš neoslovovaly. Je u nich obtížné provést klasickou, solidní analýzu založenou na kvartálních výsledcích, a stejně tak nelze objektivně posoudit kvalitu produktu nebo služby, protože často netušíme, zda výzkum vůbec někdy dospěje do zdárného konce. Člověk si připadá trochu jako ve slepé uličce, prostě do ní vkročíte a doufáte, že někam vede.
Nedávno jsem však narazil na biotechnologickou firmu, která si nečekaně získala mou pozornost, ať už svou výzkumnou příležitostí, softwarem, managementem, nebo svou konkurenční pozicí. Jsem přesvědčen, že nabízí velmi zajímavý profil rizika a výnosu.
Níže se pouštím do detailní analýzy této společnosti, která je výsledkem téměř měsíčního rešeršování. Tento text je výhradně mou vlastní prací a slouží primárně jako osobní deník odrážející mé názory a poznámky.
Disclaimer: Nemohu zaručit přesnost ani aktuálnost zde uvedených informací. Tento článek nepředstavuje finanční poradenství, investiční doporučení ani faktický základ pro vaše investiční rozhodnutí. Proveďte prosím vlastní due diligence.
Relay Therapeutics – Přehled společnosti
Relay Therapeutics je biotechnologická společnost ve fázi klinického vývoje, která se profiluje jako lídr v oblasti Tech-Bio, na průsečíku výpočetních technologií a biologie. Její hlavní konkurenční výhoda spočívá ve vlastním systému Dynamo™, který využívá umělou inteligenci (AI/ML) a molekulární dynamiku k analýze pohybu proteinů.
Budoucnost společnosti v tuto chvíli visí na jejím hlavním aktivu, léku RLY-2608. Jedná se o inhibitor PI3Kα určený k léčbě rakoviny prsu. RLY-2608 byl navržen tak, aby byl vysoce selektivní a vyhnul se toxicitě spojené s léky dřívějších generací. V současné době prochází klíčovou fází 3 klinického testování (studie ReDiscover-2).
Z finančního hlediska se společnost pyšní silnou rozvahou (cca 596 milionů USD v hotovosti ke 3. čtvrtletí 2025), což jí zajišťuje hotovostní runway (financování provozu) až do roku 2029.
Historie společnosti
Kapitola 1: Sňatek křemíku a biologie (2015–2016)
Příběh Relay Therapeutics nezačal v mokré laboratoři plné pipet, ale v serverovně. Psal se rok 2015 a biotechnologická scéna zažívala bezprecedentní konvergenci dvou odlišných světů. Na jedné straně stála společnost Third Rock Ventures, investiční firma proslulá svou schopností budovat biotechnologické firmy od nuly. Na straně druhé stála D. E. Shaw Research, vedená miliardářem a počítačovým vědcem Davidem E. Shawem. Shaw byl posedlý myšlenkou, že biologie je v jádru jen velmi složitá fyzika, kterou lze spočítat, pokud máte dostatečný výpočetní výkon.
V srdci této rodící se firmy nestál konkrétní kandidát na lék, ale superpočítač jménem ANTON. Do té doby farmaceutický průmysl vnímal proteiny, základní stavební kameny nemocí – jako statické sochy. Vědci pořídili snímek proteinu (pomocí rentgenové krystalografie) a pokoušeli se navrhnout lék, který by do něj zapadl jako klíč do zámku. Zakladatelé Relay však věděli, že proteiny nejsou sochy; jsou to neustále se pohybující stroje. ANTON byl sestrojen tak, aby místo statických snímků generoval filmy molekulárního pohybu. Právě schopnost vizualizovat to, co se děje, když je protein v pohybu, se stala základní výhodou, na které byla společnost Relay postavena.
Kapitola 2: Ve stínu miliard a hledání identity (2016–2018)
Prvních osmnáct měsíců fungovala společnost v přísném utajení (stealth mode). Teprve v září 2016 vystoupila ze stínu, vyzbrojena 57 miliony dolarů v seed kapitálu a odvážným tvrzením: že dokáže vyvinout léky na cíle, které byly dosud považovány za léky nezasažitelné (undruggable targets).
Následující dva roky byly definovány horečným budováním týmu schopného překlenout propast mezi suchou laboratoří (výpočty) a mokrou laboratoří (chemie a biologie). Bylo nezbytné dokázat, že to, co ANTON simuluje na obrazovce, odpovídá biologické realitě uvnitř lidského těla.
Zlomový okamžik pro vnímání společnosti přišel v roce 2018. Do hry vstoupil SoftBank Vision Fund, který vedl ohromující investiční kolo série C v hodnotě 400 milionů dolarů. V té době šlo o naprosto mimořádnou částku pro firmu, která neměla v klinických zkouškách jediný lék. Tato investice však vyslala trhu jasný signál: investoři nevnímali Relay jako tradiční farmaceutickou firmu, ale jako technologickou společnost (TechBio), od níž očekávali exponenciální škálovatelnost podobnou softwarovým firmám.
Kapitola 3: Zrození Dynama a vstup na burzu (2019–2020)
S příchodem roku 2019 a nového generálního ředitele Sanjiva Patela, zkušeného stratéga z Allerganu, zahájila společnost transformaci z vědeckého inkubátoru na komerční subjekt. Bylo jasné, že k úspěchu na veřejných trzích potřebuje firma srozumitelný příběh. Složitá technická vysvětlení molekulární dynamiky a superpočítačů byla pro průměrného investora-generalistu příliš abstraktní.
Aby Relay tento příběh vybudovala, musela dokázat, že je skutečnou technologickou společností, nikoliv jen tradičním vývojářem léků. Tento rozdíl se odrazil i v náborové strategii. Management často zdůrazňoval, že nehledá standardní IT pracovníky z farmacie, kteří by jen udržovali servery v chodu. Místo toho přetahovali talenty přímo od technologických gigantů jako Google či Meta. Potřebovali inženýry schopné kódovat složité simulace a zajistit, aby výpočetní tým seděl u stolu jako rovnocenný partner biologů.
Tato fúze technologií a biologie vykrystalizovala během příprav na IPO v červenci 2020, kdy došlo k formálnímu pojmenování platformy Dynamo™. Vedení potřebovalo elegantní název pro svůj unikátní pracovní postup: experimentální data krmí počítač, počítač provádí simulace pro návrh sloučeniny, ta je následně syntetizována a otestována, a výsledky se vrací zpět do systému pro další učení.
Dynamo se stalo marketingovým ztělesněním tohoto efektivního cyklu. IPO bylo triumfem; společnost vybrala stovky milionů dolarů a cena akcií vylétla vzhůru na vlně nadšení pro digitální revoluci v biologii.
Kapitola 4: Od simulací k realitě (2020–2023)
Po euforii z IPO nastal čas dospět. Relay musela prokázat, že výkon jejích superpočítačů dokáže generovat víc než jen pěkné vizualizace. Prvním velkým důkazem bylo strategické partnerství s průmyslovým obrem Genentech (součást skupiny Roche) v roce 2020 ohledně léku RLY-1971. Genentech zaplatil desítky milionů dolarů v hotovosti předem, což průmysl interpretoval jako jasnou externí validaci: „Big Pharma“ uvěřila, že tato technologie funguje.
Tento obchod však také ukázal volatilitu sektoru. V prosinci 2022 Genentech spolupráci z blíže nespecifikovaných strategických důvodů v podstatě ukončil a práva na RLY-1971 vrátil zpět Relay. Ačkoliv se dlouhodobé komerční milníky rozplynuly, počáteční partnerství splnilo svůj klíčový účel: dokázalo, že věda společnosti Relay stojí za to, aby „Big Pharma“ vytáhla šekovou knížku.
Ještě hmatatelnější ukázka schopností Dynama přišla s vývojem léku RLY-4008 (Lirafugratinib) pro cholangiokarcinom (rakovinu žlučových cest). Konkurenční léky v minulosti selhávaly kvůli problémům s toxicitou, které pramenily z neschopnosti rozlišit mezi dvěma strukturálně podobnými receptory (FGFR1 a FGFR2).
Díky simulaci pohybu identifikovala Relay v receptoru FGFR2 tzv. skrytou kapsu (cryptic pocket), která se otevírá jen na zlomek vteřiny. Následně navrhli molekulu, která se váže výhradně na toto přechodně dostupné místo. V ten moment se teorie proměnila v klinickou realitu, Dynamo vyřešilo problém selektivity, který tradiční medicinální chemii dlouho unikal.
Kapitola 5: Strategická dospělost (2024–současnost)
Relay Therapeutics v současnosti vstupuje do nové éry. Už to není ten startup s velkými sny, který chce prozkoumat každou hranici biologie. V reakci na požadavky trhu na kapitálovou efektivitu a jasnou cestu k ziskovosti musel management učinit pragmatická rozhodnutí.
Na konci roku 2024 společnost poskytla licenci (out-licensing) na svůj úspěšný program RLY-4008 externímu partnerovi. Tento strategický krok měl za cíl uvolnit provozní kapacity a přesměrovat kapitál k aktivu, o němž je firma nejvíce přesvědčena: k léku RLY-2608 na rakovinu prsu.
Příběh se tak uzavírá v kruhu. Od teoretických simulací na superpočítači ANTON v roce 2015 se společnost vyvinula do bodu, kdy sází svou budoucnost na potenciální blockbuster; lék s ambicí redefinovat standard péče (SoC) u jedné z nejrozšířenějších forem rakoviny.
Platforma Dynamo™: Unikátní konkurenční výhoda
Vše začalo vývojem softwarové platformy Dynamo™. Vědci po celá desetiletí vyvíjeli léky na základě statických modelů, představte si to, jako byste analyzovali jedinou fotografii struktury. Naproti tomu platforma Dynamo™ simuluje proteiny v pohybu, čímž v podstatě vytváří video ve vysokém rozlišení.

Využití dynamických modelů k lepšímu pochopení pohybu proteinů s cílem formulovat nové hypotézy pro inhibici cíle. (Zdroj: Relaytx.com)
Tento přístup zdokonaluje tradiční teorii zámku a klíče při vývoji léků. Aby byl lék účinný, musí molekula nejen zapadnout do proteinového zámku, ale musí zůstat pevně navázaná i ve chvíli, kdy se protein hýbe a mění svůj tvar.
Systém integruje vysoce výkonné výpočty (HPC), simulace AI/ML založené na fyzikálních principech a experimentální data, aby zmapoval celý konformační prostor proteinů. Tento dynamický pohled odhaluje zásadní rozdíl: zatímco zdravý zámek (protein) zůstává často pevný a stabilní, rakovinotvorná mutace fluktuuje a vibruje.
Společnost Relay tento poznatek využívá k navrhování léků, které přesně zapadnou právě do těchto přechodně otevřených kapes. Výsledkem je terapie, která účinně cílí na rakovinu, zatímco zdravou tkáň nechává nedotčenou.
RLY-2608
Mechanismus účinku (MoA) a technologická inovace
Toto výzkumné aktivum představuje inhibitor PI3Kα nové generace, který se od předchozích terapií zásadně odlišuje unikátním způsobem vazby. Zatímco konvenční léky cílí na ortosterické místo (aktivní centrum enzymu), což je přístup často přirovnávaný k použití hrubé síly – RLY-2608 využívá alosterickou inhibici.
S využitím platformy Dynamo identifikovala Relay specifickou konformační změnu, metaforicky řečeno tajnou štěrbinu či skrytou kapsu, která se vyskytuje výhradně u zmutované formy proteinu PI3Kα. Lék se váže pouze na toto místo, čímž efektivně uzamyká mutantní protein v neaktivním stavu, aniž by narušil funkci zdravého (wild-type) proteinu.
Srovnání se standardem péče (SoC) a řešení toxicity
Současná léčba karcinomu prsu s mutací PI3Kα je definována ostrým kompromisem mezi účinností a závažnou toxicitou. RLY-2608 tento model mění díky své extrémní selektivitě.
- Výzva spojená s hyperglykemií (Alpelisib/Inavolisib): Zdravý (wild-type) protein PI3Kα hraje klíčovou roli v inzulinové signalizaci. Zavedené léky jako alpelisib (Piqray) a v menší míře i inavolisib (Itovebi) nechtěně zasahují i tento zdravý protein (tzv. off-target efekt), což vede k narušení metabolismu glukózy. Výsledkem je vysoká míra hyperglykemie, která postihuje až 60 % pacientů užívajících alpelisib. To si vynucuje přísná dietní omezení, nasazení antidiabetik nebo úplné vysazení léčby. RLY-2608 tím, že zdravý protein efektivně ignoruje, vykazuje v klinických datech zanedbatelný výskyt hyperglykemie.
- Výzva spojená s gastrointestinální (GI) toxicitou (Capivasertib): Konkurenční inhibitor AKT, capivasertib (Truqap), způsobuje průjem u více než 70 % pacientů. Tyto příhody jsou často závažné a vedou k nutnému snižování dávek či přerušování terapie. RLY-2608 tento vysilující profil toxicity nevykazuje.
Klinický přínos a řešení nenaplněných potřeb
Hlavní hodnotovou propozicí RLY-2608 je potenciál udržet setrvalou intenzitu dávkování. V onkologii je terapeutická účinnost neoddělitelně spjata s adherencí (dodržováním léčby). Je kriticky důležité, aby pacienti zůstali na plném léčebném režimu dlouhodobě, bez nucených přerušení nebo lékových prázdnin vyvolaných nesnesitelnými vedlejšími účinky.

Zdroj: Firemní prezentace Relay Therapeutics, listopad 2025
Výsledky 1. a 2. fáze klinické studie (Re-Discover)
Data ze studie ReDiscover poskytla přesvědčivé důkazy o vysoké účinnosti RLY-2608 u silně předléčené populace pacientek.
Klíčovým měřítkem úspěchu je medián přežití bez progrese (mPFS). Při dávce 600 mg dosáhl mPFS v celkové populaci 10,3 měsíce a u pacientek v tzv. čisté druhé linii (clean second-line setting) dokonce 11,0 měsíce. Tato čísla představují dramatické zlepšení oproti historickým benchmarkům konkurence u srovnatelných populací, kde se léky jako capivasertib nebo alpelisib typicky pohybují pouze v rozmezí 5,5 až 7,1 měsíce. RLY-2608 tak efektivně zdvojnásobuje dobu kontroly nad onemocněním.
Objektivní zmenšení nádoru a klinický benefit
Kromě pouhé stabilizace nemoci lék prokázal schopnost aktivně snižovat nádorovou zátěž. Míra objektivní odpovědi (ORR) dosáhla 39 %, což výrazně překonává hodnoty pozorované u konkurenčních látek v podobných studiích (např. 19 % u inavolisibu a 26 % u capivasertibu).
Míra klinického benefitu (CBR), která zahrnuje i stabilizované onemocnění, byla zaznamenána na úrovni 67 %. Tato čísla potvrzují, že mechanismus alosterické inhibice není jen teoretickým konceptem, ale promítá se do hmatatelné, měřitelné regrese nádoru.
Diferenciace v toxicitě a metabolická bezpečnost
Kritickým poznatkem z dat fáze 1 je validace hlavní hypotézy: selektivita vůči mutantnímu proteinu eliminuje metabolická rizika typická pro tuto třídu léků.
Na rozdíl od inhibitorů dřívějších generací (alpelisib) nebo degradérů (inavolisib) nevykazuje RLY-2608 žádný významný výskyt závažné hyperglykemie, protože nezasahuje do inzulinové dráhy zprostředkované wild-type proteinem. Studie neukázala potřebu složitého monitorování glukózy ani profylaktického podávání antidiabetik, což výrazně zlepšuje kvalitu života pacientů a komfort léčby.
Absence hepatotoxicity a GI tolerance
V kontextu konkurenčního prostředí je zásadní absence signálů jaterní toxicity (hepatotoxicita). Tento problém trápil jiné molekuly vyvíjené v této třídě, například ty od Scorpion Therapeutics.
RLY-2608 byl dobře snášen i při plných terapeutických dávkách bez negativního dopadu na jaterní enzymy. Pacienti navíc netrpěli průjmy limitujícími dávku v takovém rozsahu, jaký je pozorován u capivasertibu. Tato kombinace „čistého“ bezpečnostního profilu umožňuje pacientům setrvat na léčbě déle a v plném dávkování, což přímo koreluje s lepšími výsledky přežití.

Zdroj: Firemní prezentace Relay Therapeutics, listopad 2025
Klíčová fáze 3 studie RLY-2608: Re-Discover 2 (2025)
Společnost Relay Therapeutics vstoupila zahájením své registrační studie fáze 3, ReDiscover-2, do kritického bodu svého firemního životního cyklu. Tato studie představuje vyvrcholení let výzkumu a vývoje na platformě Dynamo a jejím cílem je definitivně validovat terapeutický potenciál RLY-2608, mutant-selektivního inhibitoru PI3Kα.
Studie je navržena jako přímé srovnání (head-to-head) proti současnému standardu péče (SoC) v druhé linii léčby metastatické rakoviny prsu: kombinaci léku capivasertib a fulvestrant. Úspěch v této studii není jen otázkou vědecké prestiže; je to definitivní katalyzátor pro komerční budoucnost společnosti a pro její potenciální atraktivitu jakožto akvizičního cíle pro strategické partnery.
Design studie a metodika
ReDiscover-2 je strukturována jako globální, multicentrická, randomizovaná klinická studie s otevřeným uspořádáním (open-label). Ačkoliv open-label design znamená, že lékaři i pacienti vědí, jaká léčba jim byla přidělena, objektivita primárního cíle (endpointu) je rigorózně chráněna procesem zaslepeného nezávislého centrálního hodnocení (BICR). To zajišťuje, že snímky z vyšetření vyhodnocují nezávislí radiologové, kteří nemají tušení, do kterého léčebného ramene pacient patří.
Cílem je prokázat, že RLY-2608 nabízí nejen srovnatelný či lepší čas do progrese onemocnění (PFS), ale – a to je klíčové – výrazně lepší bezpečnostní profil. Tedy profil oproštěný od toxicit limitujících dávku, jako jsou hyperglykemie a silné průjmy, které sužují konkurenční terapie.
Geografická alokace a náborová strategie
Klíčovým poznatkem z analýzy operačního plánu je strategické rozložení populace pacientů. Z celkového plánovaného náboru 540 pacientů zvolila Relay vyvážený, mírně eurocentrický přístup. Přibližně polovina účastníků (272 pacientů) má být rekrutována z evropských center, zatímco zbývajících 268 připadá na zbytek světa (RoW), jemuž dominují USA a klíčové asijské trhy.
Tato alokace naznačuje soustředěnou snahu o maximalizaci rychlosti náboru a zajištění diverzifikace dat, což je nezbytné pro globální regulatorní podání (schvalování léku úřady v různých zemích).
Má osobní vsuvka: Česká stopa
Zajímavostí je, že Česká republika hraje v této evropské části studie významnou roli. Byla identifikována jako aktivní účastník a zapojení osmi špičkových pracovišť (včetně Masarykova onkologického ústavu v Brně a fakultních nemocnic v Praze a Olomouci) podtrhuje důraz, jaký je kladen na kvalitu dat.

Veřejně dostupná data Evropské agentury pro léčivé přípravky (EMA). Zdroj: euclinicaltrials.eu
Detailní plánování, které počítá s náborem přibližně jedenácti pacientů z těchto českých center, přispívá do širší mozaiky celé studie. Střední Evropa je historicky uznávána pro vysokou motivaci pacientů a striktní dodržování klinických protokolů (adherenci), což přidává očekávaným datům další vrstvu spolehlivosti.
Provozní infrastruktura a kontrola kvality
K realizaci projektu takového rozsahu se Relay Therapeutics rozhodla spojit s absolutní špičkou v oboru (best-in-class partnery), čímž minimalizuje riziko selhání exekuce. Celkové řízení studie bylo svěřeno společnosti IQVIA, globálnímu lídrovi mezi smluvními výzkumnými organizacemi, což garantuje bezproblémovou logistiku a monitoring.
Úhelným kamenem vědecké validity je zapojení Foundation Medicine, která zajišťuje precizní genetické testování a přesný výběr pacientů nesoucích specifickou mutaci. Na sběr dat a jejich integritu dohlíží technologický gigant Medidata Solutions, zatímco proplácení nákladů pacientům a plynulost plateb řídí systém Greenphire.
Tato sestava dodavatelů, zahrnující i specializované firmy na logistiku léků a farmakovigilanci, vysílá investorům jasný signál: společnost je dobře kapitalizovaná a odmítá dělat kompromisy v kvalitě dat tím, že by šetřila na nesprávných místech.
Klíčový konkurent: STX-478 od Scorpion Therapeutics
Strategická akvizice a validace technologie
Vstup farmaceutického giganta Eli Lilly do arény skrze akvizici programu STX-478 (nyní pod označením LY4064809) v celkové hodnotě až 2,5 miliardy dolarů představuje pomyslnou dvousečnou zbraň.
Na jedné straně tento krok validuje obrovskou hodnotu a vědeckou tezi alosterické inhibice PI3Kα – tedy přesně tu sázku, kterou činí i Relay. Na straně druhé to staví Relay do pozice Davida proti Goliášovi, kdy proti ní stojí konkurent s prakticky neomezenými zdroji na marketing a klinický vývoj. Tato akvizice je jasným signálem, že Big Pharma vnímá selektivní inhibici jako budoucnost tohoto oboru.
Klinické výhody a diferenciace STX-478
Hlavní konkurenční výhoda STX-478 spočívá v jeho farmakokinetickém profilu, který umožňuje dávkování jednou denně (QD). To představuje mírnou výhodu v pohodlí pro pacienta oproti režimu dvakrát denně (BID), který vyžaduje RLY-2608.
Potenciálně mnohem významnějším benefitem je však schopnost molekuly překonat hematoencefalickou bariéru (CNS penetrace). To by mohlo zajistit dominanci STX-478 v podskupině pacientek s mozkovými metastázami, v oblasti, kde mají současné terapie (a pravděpodobně i RLY-2608) omezenou účinnost. Pokud se tato schopnost potvrdí v klinických studiích, Eli Lilly by mohla efektivně obsadit a ovládnout tento specifický, leč kritický tržní segment.
Bezpečnostní rizika a hepatotoxicita
Navzdory silnému zázemí však program STX-478 čelí významným bezpečnostním otazníkům. Data prezentovaná na velkých lékařských konferencích (např. ESMO) odhalila signály hepatotoxicity (jaterní toxicity), manifestující se zvýšením jaterních enzymů (ALT/AST), zejména při vyšších dávkách.
Ačkoliv jde o data z rané fáze, potenciální nutnost snižování dávek kvůli bezpečnosti by mohla ohrozit celkovou účinnost léku. V ostrém kontrastu s tím nevykazuje RLY-2608 doposud žádné signály hepatotoxicity, což mu dává klíčovou konkurenční výhodu v závodě o to stát se „nejčistším“ lékem ve své třídě.
Výhoda „Time-to-Market“
Zatímco Eli Lilly po akvizici stále integruje program do svých struktur a nachází se ve fázi 1/2 vývoje (studie Pikalo-2), Relay Therapeutics již aktivně nabírá pacienty do své registrační fáze 3 (ReDiscover-2).
Tato výhoda prvního tahu v rámci třídy léků nové generace je kritická. Umožňuje Relay etablovat se jako nový standard péče (SoC) dříve, než Eli Lilly dokončí své studie, a dává jí tak časové okno k definování trhu – zejména pokud jde o vnímání bezpečnosti a metabolické snášenlivosti.
Válka o druhou linii: Historie toxických kompromisů
Kontext konkurenčního prostředí a chronologický vývoj terapií HR+/HER2-
Dovolte mi odvyprávět krátký historický příběh, který odráží to, co vnímám jako doslovné podmínky na bojišti v zápase o pacienty.

Kapitola I: Úsvit nové éry a dominance Pfizeru (2015–2017)
Píše se rok 2015. Do té doby léčba metastatického karcinomu prsu (HR+/HER2-) spoléhala primárně na endokrinní (hormonální) terapii, která však často selhávala příliš brzy. Pfizer do této stagnace vtrhl jako absolutní průkopník. Představil Ibrance (palbociclib), první inhibitor CDK4/6 na světě, který cílil na buněčný cyklus. Fungoval tak dobře, že se okamžitě stal novým zlatým standardem pro léčbu v 1. linii (1L).
Pfizer ovládl celý trh a Ibrance se stal synonymem moderní onkologie. Konkurence však nespala. Trvalo to dva roky, ale v roce 2017 se na bojišti objevili dva vyzyvatelé. Eli Lilly uvedla na trh Verzenio a Novartis přišel s lékem Kisqali.
Ačkoliv dorazili se zpožděním, přinesli vylepšení. Zatímco Ibrance nemoc pouze zpomaloval (Progression-Free Survival), Kisqali a Verzenio v pozdějších studiích prokázaly, že díky nim pacienti skutečně žijí déle (benefit v celkovém přežití / Overall Survival). Tito tři císaři si rozdělili trh první linie, ale Pfizer díky své výhodě prvního tahu stále držel korunu.
Kapitola II: Temná ulička druhé linie a toxická daň (2019–2023)
S postupem let se objevil nový problém. Rakovina je inteligentní; časem si vyvine rezistenci vůči lékům první linie, často hnanou mutací genu PI3K. Pacienti zoufale potřebovali nový lék, který by zabral ve chvíli, kdy Ibrance selže.
V roce 2019 zvedl hozenou rukavici Novartis a uvedl Piqray (alpelisib), první cílený inhibitor PI3K. Byl to vědecký triumf, ale pro pacienty to bylo Pyrrhovo vítězství. Piqray byl tzv. špinavý lék (dirty drug). Zasahoval do metabolismu glukózy tak drasticky, že u mnoha žen vyvolal okamžitou a těžkou cukrovku. Lékaři jej předepisovali se zdráháním. Byla to volba mezi smrtí na rakovinu, nebo životem v metabolickém pekle.
Této slabiny využila AstraZeneca. V roce 2023 představila Truqap (capivasertib). Zamířili o krok vedle (zacílili na protein AKT) a slíbili lepší snášenlivost. Podařilo se jim vyřešit problém s cukrovkou, ale vyměnili ho za jiný: silné, vysilující průjmy. Přesto to znamenalo pokrok a Astra začala přebírat otěže v nastavení druhé linie.
Kapitola 3: Šok jménem Roche a pád bariér (2024)
Zatímco se Novartis a AstraZeneca praly o zbytky ve druhé linii, švýcarský gigant Roche tiše připravoval převrat. Rozhodli se ignorovat dogma, že inhibitory PI3K patří až na úplný konec léčebného řetězce, a provedli to s dravostí, která zaskočila i samotný Pfizer.
V roce 2024 Roche šokovala svět. Odhalila Inavolisib, molekulu fungující jako degradér proteinu PI3K. Pro svou klíčovou studii si jako partnera zvolili starý dobrý Ibrance (palbociclib). Na tom by nebylo nic zvláštního, kdyby šlo o spolupráci. Jenže Roche se nikoho neptala. Využili faktu, že Ibrance je veřejně dostupným standardem péče (SoC), a bez jakékoli strategické dohody či svolení Pfizeru jej použili jako nosič pro svůj vlastní úspěch.
Pfizer byl nucen stát stranou a sledovat, jak Roche využívá jejich vlastní lék k dobytí trhu, který jim proklouzával mezi prsty. Pro Roche to byl geniální tah, navíc oslazený vědomím, že patentová ochrana Ibrance začíná v roce 2027 vyprchávat, což jim v budoucnu umožní využít levné generické verze a stlačit náklady na tuto vítěznou kombinaci na minimum.
Výsledek byl revoluční. Prokázali, že nasazení této trojkombinace (tripletu) okamžitě v 1. linii (1L) přidává pacientkám měsíce života navíc. Poprvé v historii lék cílící na tuto mutaci prolomil bariéru první linie. Roche přeskočila veškerou konkurenci a nastavila laťku účinnosti brutálně vysoko.
Pro Pfizer to byla studená sprcha, která měla devastující dopad na jejich interní plány. V té době měli (a stále mají) v pokročilém vývoji (fáze 3) svého vlastního korunního prince, atirmociclib, navržený jako náhrada za Ibrance. Plánem bylo jej v tichosti uvést jako vylepšenou verzi starého léku. Úspěch Roche však změnil pravidla hry uprostřed zápasu. Pfizer si uvědomil, že v novém světě, kde je inhibice PI3K standardem od prvního dne, nedává design jejich původní studie smysl. Museli učinit to nejbolestivější rozhodnutí ve vývoji léků: zatáhnout za záchrannou brzdu, přehodnotit studie a kompletně překopat jejich design, aby měli vůbec šanci bojovat.
Mělo to však háček. Ačkoliv Inavolisib od Roche fungoval výborně, stále si vybíral svou daň, stomatitidu (boláky v ústech) a záněty sliznic, umocněné potlačením imunity ze strany Ibrance. Byla to účinná, ale bolestivá léčba. A právě to dalo Pfizeru čas a důvod hledat nového partnera.
Kapitola IV: Závody ve zbrojení a honba za dokonalostí (Současnost – 2025)
Úspěch Roche vyslal vlnu paniky do zasedaček konkurence. Eli Lilly, Pfizer i Novartis si uvědomili stejnou tvrdou pravdu: pokud do první linie nepostaví svůj vlastní triplet, Roche je prakticky vymaže z mapy.
Hon na čisté látky začal. Eli Lilly zareagovala okamžitě a agresivně. V lednu 2025 zajistila práva na program STX-478 od Scorpion Therapeutics, aby si pojistila vlastní inhibitor PI3K a spárovala jej se svým inhibitorem CDK4/6, Verzeniem.
Pfizer, sledující ústup svého stárnoucího krále Ibrance, vsadil vše na vývoj aktiva nové generace: atirmociclibu. Tento lék funguje jako odstřelovač: ničí rakovinu (CDK4), zatímco šetří krev (CDK6), čímž se vyhýbá problémům s neutropenií, které trápily jeho předchůdce. Přesto i Pfizer věděl, že samotný atirmociclib nebude na zastavení Roche stačit. Potřebovali partnera.
A Novartis? Ten se ocitl v nejprekérnější pozici. Jejich klenot, Kisqali, potřeboval ochranu, ale jejich vlastní aktivum, Piqray, bylo pro tento účel kvůli své toxicitě nepoužitelné.
Kapitola V: Naděje jménem Relay (Budoucnost?)
Uprostřed tohoto chaosu a zběsilého zbrojení se zraky všech stočily k malé firmě z Cambridge: Relay Therapeutics.
Jejich aktivum, RLY-2608, vykované superpočítačem Dynamo, se ukázalo být přesně tím, co všichni hledali. Byl to onen pomyslný svatý grál: lék, který cílil na mutaci se stejnou razancí jako Inavolisib, ale díky své chirurgické přesnosti se vyhýbal toxické triádě: cukrovce, stomatitidě a průjmům.
Pfizer i Novartis pochopili, že RLY-2608 je klíčem k poražení Roche. Došlo tak k bezprecedentní události: ještě před dokončením finálních testů začali oba giganti společnosti Relay nadbíhat. Spustili klinické studie, v nichž testují svá nejlepší aktiva (Kisqali a atirmociclib) v trojkombinaci (tripletu) specificky s RLY-2608.
Cíl je jasný: Vytvořit super-čistý triplet. Léčebný režim stejně účinný jako ten od Roche, ale takový, který mohou pacientky užívat roky bez utrpení.
Relay Therapeutics tak stojí v epicentru celého odvětví. S lékem, který má potenciál přepsat historii, a se dvěma multimiliardovými nápadníky, kteří vědí, že ten, kdo získá RLY-2608, pravděpodobně vyhraje válku o budoucnost léčby rakoviny prsu, minimálně pro několik příštích let.
Corporate Governance a strategická restrukturalizace
Vedení společnosti: Od vědy k transakci
V čele společnosti stojí tým, který snoubí hlubokou vědeckou expertízu s pragmatismem velkého byznysu. Ústřední postavou je Dr. Sanjiv Patel, prezident a CEO. Jeho profil je jako šitý na míru současné fázi firmy: jako bývalý chirurg chápe klinickou realitu, ale jako někdejší ředitel pro strategii (CSO) v Allerganu (kde hrál klíčovou roli v multimiliardových fúzích) má myšlení investičního bankéře. Není to akademický vizionář, ale exekutivní manažer s laserovým zaměřením na maximalizaci hodnoty.
Sekunduje mu Dr. Don Bergstrom (prezident výzkumu a vývoje), který přináší rozsáhlé zkušenosti od velkých farmaceutických hráčů (Sanofi, Merck). Jeho background je zárukou, že vygenerovaná klinická data obstojí pod drobnohledem regulátorů i potenciálních kupců.
Představenstvo: „Dream Team“ pro exitovou strategii
Složení představenstva (Board of Directors) slouží jako nejsilnější signál, že se Relay připravuje na velkou strategickou transakci. Nejde o pasivní dozorčí orgán, ale o sbírku architektů úspěšných exitů:
- Alexis Borisy (předseda): Sériový podnikatel, který úspěšně vybudoval a prodal Foundation Medicine společnosti Roche za 5,3 miliardy dolarů. Jeho přítomnost zajišťuje přímý přístup do nejvyšších pater (C-suite) Big Pharmy.
- Dr. Krishna Yeshwant (Google Ventures): Zástupce technologického kapitálu, General Partner v GV a praktikující lékař. Jeho role validuje technologické základy platformy Dynamo a udržuje most do Silicon Valley a AI ekosystému, na němž byla Relay založena.
- David E. Shaw: Otec superpočítače ANTON, který firmě zajišťuje technologickou unikátnost a obhajitelnou konkurenční výhodu.
- Habib Dable a Lonnel Coats: Nedávno jmenovaní členové, kteří přinášejí specifické know-how v oblasti komercializace a fúzí a akvizic (M&A). Za zmínku stojí zejména Dable, který zrežíroval prodej společnosti Acceleron do rukou Mercku za 11,5 miliardy dolarů.
Poznámka: Spojení s Googlem
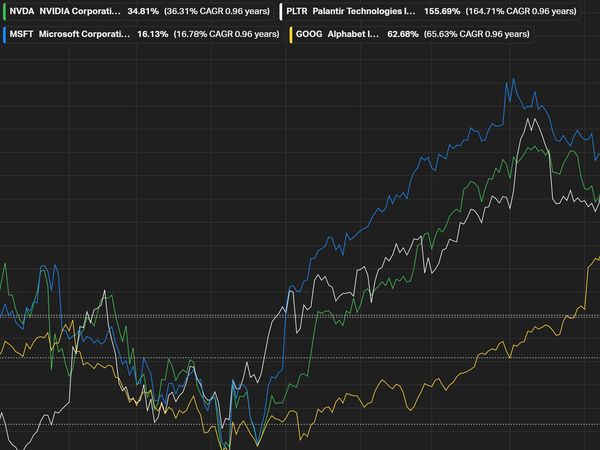
Když už mluvíme o Dr. Yeshwantovi, je tu jeden málo známý fakt: Google jen nepřihlíží z postranní čáry. Alphabet (skrze GV) firmu podporuje od prvního dne a stále drží (k Q3 2025) významnou pozici ve výši 1 568 753 akcií. Jde o tichý, ale silný hlas důvěry v AI schopnosti Relay.

Zdroj: WhaleWisdom.com
Restrukturalizace: „Strojení nevěsty“
V uplynulém roce prošla Relay Therapeutics zásadní a bolestivou transformací, krokem typickým pro firmy chystající se na akvizici. Společnost propustila přibližně 10 % zaměstnanců a zastavila nákladné projekty v rané fázi (jako byl interní vývoj Lirafugratinibu), které nebyly kritické pro okamžitou tvorbu hodnoty.
Cílem této čistky bylo snížit pálení hotovosti (cash burn) a koncentrovat veškeré zdroje na korunní klenot: RLY-2608. Management tím prodloužil hotovostní runway až do roku 2029 a vytvořil štíhlou, efektivní strukturu, která je pro potenciálního kupce vysoce atraktivní, jelikož po akvizici nebude nutné ořezávat tolik organizačního tuku.
Strategický kontext: Pfizer jako logický přístav
Všechny výše zmíněné kroky, od složení představenstva po finanční disciplínu, směřují k jedinému cíli: učinit z Relay neodolatelný akviziční cíl. Zatímco Novartis zůstává potenciálním nápadníkem (byť třeba jen z defenzivních důvodů, aby chránil svou franšízu Kisqali), Pfizer se jeví jako nejlogičtější přístav.
Už jen fakt, že aktuálně běží studie testující specifickou trojkombinaci, podpořená dohodou o sdílení dat (která dává Pfizeru v podstatě nahlédnout pod kapotu v reálném čase), naznačuje zájem na nejvyšší úrovni. Po nuceném resetu své vlastní studie s atirmociclibem Pfizer zoufale potřebuje partnera pro čistou kombinační terapii, aby mohl čelit agresivnímu postupu Roche.
Společné testování (atirmociclib + RLY-2608), personální propojení a technologická kompatibilita, to vše naznačuje, že Relay projektuje svou budoucnost tak, aby dokonale zapadla do onkologického portfolia Pfizeru jako onen chybějící dílek skládačky.
Rozšíření pipeline: Cévní malformace
Odemknutí nových trhů za hranicemi onkologie
Kromě rakoviny prsu otevírá molekula RLY-2608 dveře k léčbě vzácných, ale invalidizujících genetických poruch cévního systému, souhrnně známých jako cévní malformace (VM). Tato onemocnění jsou často způsobena naprosto stejnou mutací genu PIK3CA, na kterou lék cílí v onkologii.
Současný standard péče (SoC) je tristní. Jediná schválená terapie, alpelisib (prodávaný Novartisem pod názvem Vijoice), nedávno nesplnila primární cíl v potvrzující studii EPIK-P2. Jeho účinnost byla nepřesvědčivá (ORR 17–23 %) a jeho toxický profil, charakteristický hyperglykemií a potlačením růstu u dětí – je pro chronickou, celoživotní léčbu, která často začíná v dětství, neakceptovatelný. Novartis tak na trhu zanechal významné terapeutické vakuum.
Vyšší účinnost a bezpečnostní profil
V předklinických modelech Relay Therapeutics prokázala, že RLY-2608 je v léčbě malformací výrazně účinnější než alpelisib. Zatímco alpelisib růst lézí pouze zpomaloval (cytostatický efekt), RLY-2608 vyvolal jejich hlubokou regresi (zmenšení).
Klíčovou výhodou je opět selektivita. Díky absenci metabolické toxicity (hyperglykemie) je RLY-2608 ideálním kandidátem pro dlouhodobé podávání u pediatrické populace a mladých dospělých, kde je bezpečnost absolutní prioritou.
Strategie „Pathfinder“ a komerční potenciál
Společnost zvolila velmi sofistikovanou vývojovou strategii. V roce 2025 zahájila klinickou studii s využitím RLY-2608 jako důkazu konceptu (proof of concept), aby rychle validovala, že biologický princip funguje i u lidí.
Pro finální komercializaci však plánují nasadit novou, optimalizovanou molekulu ze stejné chemické rodiny. Tento krok má dvojí strategické opodstatnění:
- Cenová segmentace: Umožňuje firmě oddělit vysokou cenovku onkologického léku od cenové struktury vyžadované pro léčbu chronických onemocnění, což optimalizuje úhradové strategie pro obě indikace.
- Prodloužení IP (duševního vlastnictví): Zavedení odlišné molekuly efektivně resetuje patentové hodiny, čímž zajistí tržní exkluzivitu a příjmy na dalších 20 let.
Průlom v NRAS a genetických onemocněních
Prolomení kódu nelečitelných cílů
Mimo pokročilou klinickou pipeline skrývá portfolio Relay další potenciální blockbuster v podobě předklinického programu zaměřeného na mutace NRAS. Tento gen byl dlouho považován za léky nezasažitelný cíl (undruggable target), jelikož historické pokusy buď postrádaly účinnost, nebo vyvolávaly neúnosnou toxicitu kvůli nechtěným zásahům (off-target efektům) na blízce příbuzné proteiny KRAS a HRAS.
RLY-8161: Chemická chirurgie
Relay Therapeutics odhalila molekulu RLY-8161, která v předklinickém testování vykazuje vysoce slibné vlastnosti. Data potvrzují, že se molekula váže silně a výhradně na zmutovaný NRAS, zatímco ostatní izoformy RAS (KRAS, HRAS) a zdravé buňky efektivně ignoruje.

Zdroj: Firemní prezentace Relay Therapeutics, listopad 2025
V animálních modelech odvozených od pacientů (PDX) lék vyvolal kompletní regresi nádorů u melanomu a trvalé potlačení růstu u kolorektálního karcinomu, tedy v oblastech, kde kandidáti konkurence často selhávají kvůli rychlému nástupu mechanismů rezistence. Díky této vynikající selektivitě je lék dobře snášen i při dávkách 10× vyšších, než jsou terapeutické hladiny, což slibuje široké terapeutické okno pro budoucí pacienty.

Zdroj: Firemní prezentace Relay Therapeutics, listopad 2025
Tržní příležitost
Tento program cílí na trh s masivní nenaplněnou lékařskou potřebou (tvoří cca 20 % melanomů a 4 % kolorektálních karcinomů), kde v současnosti neexistuje žádná schválená přímá cílená terapie.
Shrnutí
Nacházíme se v kritickém, avšak strategicky fascinujícím bodě životního cyklu této společnosti. Akcie se obchodují poblíž historických minim, což vytváří masivní asymetrii mezi rizikem a potenciálním výnosem (reward). Jakákoliv pozitivní zpráva může posloužit jako silný katalyzátor pro prudký růst ceny.

Zdroj: TradingView
Klíčem pro nadcházející měsíce je ostražitě sledovat postup náboru do fáze 3 studie RLY-2608 a především monitorovat signály ze zákulisí. Rozhodujícím faktorem je zde informační asymetrie: strategičtí partneři (zejména Pfizer) vidí data o bezpečnosti a účinnosti z trojkombinací v reálném čase, dávno předtím, než je spatří širší trh.
Pravděpodobnost a scénáře exitu
Vzhledem k technologickému náskoku platformy Dynamo, představenstvu silně orientovanému na uzavírání transakcí (transaction-making) a zoufalé potřebě „Big Pharmy“ (Pfizer, Novartis) doplnit své onkologické pipeline, odhaduji pravděpodobnost převzetí (buyoutu) na více než 80 %.
Níže uvádím finanční rozpad dvou primárních scénářů exitu (za předpokladu odhadovaných cca 135–140 milionů akcií v oběhu):
Scénář A: Akvizice před dokončením fáze 3
- Logika: Pfizer (nebo Novartis) v průběžných datech z „namlouvací“ fáze (fáze 1/2) zjistí, že kombinace funguje perfektně. Rozhodnou se nečekat do roku 2028 a koupí firmu okamžitě, aby ušetřili na prémii a zabránili konkurenci v přebíjení nabídky.
- Valuace: 3 – 5 miliard USD
- Cílová cena na akcii: ~22 až 36 USD (Představuje potenciální upside cca 3x až 5x od současných úrovní).
Scénář B: Akvizice po úspěšné fázi 3
- Logika: Relay dokončí studii a prokáže jasnou převahu nad Truqapem a bezpečnostní profil lepší než Inavolisib. Lék se stane novým zlatým standardem a firma bude držet v rukou tzv. de-riskované (zbavené rizika) blockbuster aktivum.
- Valuace: 5 – 8 miliard USD (Zahrnuje prémii za platformu a program NRAS).
- Cílová cena na akcii: ~36 až 58 USD (Představuje potenciální upside cca 5x až 8x od současných úrovní).
Scénář C: Samostatná budoucnost
- Logika: K buyoutu nedojde a Relay bude pokračovat jako nezávislá komerční entita. Ačkoliv to vzhledem ke strategickému kontextu považuji za nepravděpodobné, zůstává to možností, kterou je třeba zahrnout do řízení rizik.
Závěr
Situace je nyní nakloněna trpělivému investorovi, který chápe hlubší souvislosti.
Kostky jsou vrženy.
22. 1. 2026 ~ Akciový Filozof
Disclaimer: Tento článek nepředstavuje finanční poradenství, investiční doporučení ani faktický podklad pro vaše investiční rozhodnutí.